Công thức cấu tạo của Etilen C2H4. Tính chất hoá học của etilen và bài tập thuộc phần: CHƯƠNG V: DẪN XUẤT CỦA HIĐROCACBON. POLIME
I. Công thức cấu tạo của Etilen C2H4
– Công thức của etilen gồm :
+ Công thức phân tử : C2H4 .
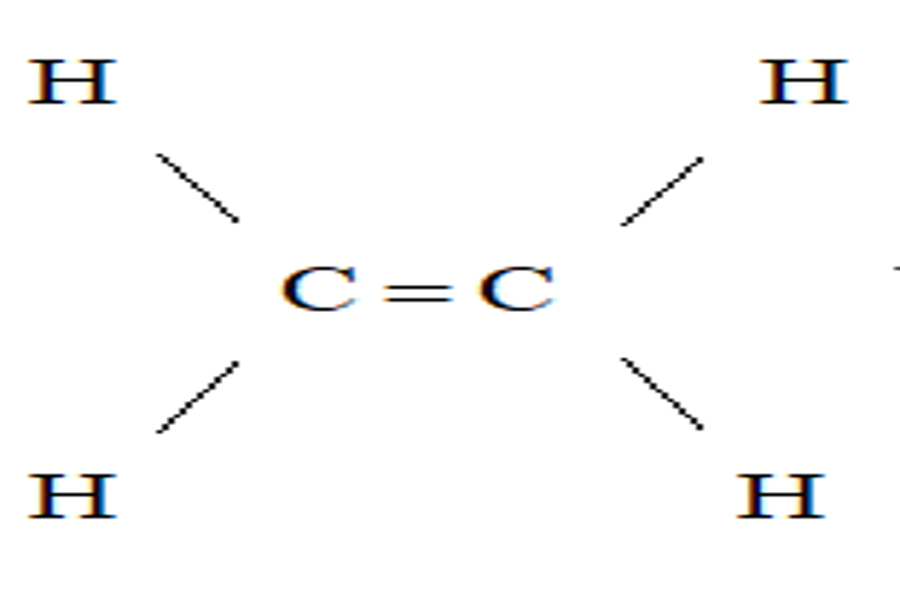
+ Công thức cấu tạo:  Viết gọn: CH2=CH2.
Viết gọn: CH2=CH2.
– Trong phân tử etilen C2H4, có một link đôi giữa hai nguyên tử cacbon .
– Trong link đôi có một link kém bền. Liên kêt này dễ đứt ra trong những phản ứng hóa học .
– Những hiđrocacbon mạch hở, trong phân tử có một link đôi như etilen gọi là anken, có công thức chung CnH2n với n ≥ 2 .
III. Tính chất hoá học của etilen C2H4
- Định nghĩa: Etilen C2H4 là một hyđrocacbon không no nằm trong dãy đồng đẳng của anken. Etilen là chất khí, không màu, không mùi, ít tan trong nước, nhẹ hơn không khí (d=28/29 ).
- Danh pháp+ Tên quốc tế: C2H4 có tên gọi là etilen+ Tên nhóm CH2=CH2- được gọi là nhóm vinyl.
Etilen C2H4 Tác dụng với oxi:
– Khi đốt trong oxi, etilen cháy tạo thành khí CO2 và H2O, tỏa nhiều nhiệt .
C2H4 + 3O2  2CO2↑ + 2H2O
2CO2↑ + 2H2O
Etilen C2H4 tác dụng với dung dịch Brom
– Dung dịch Brom hay nước Brom có màu vàng da cam ; Ở phản ứng này, một link kém bền trong link dôi bị đứt ra và phân tử etilen phối hợp thêm một phân tử brom. Phản ứng trên gọi là. hàn ứng cộng .
CH2 = CH2 + Br2 ( dd ) → Br-CH2-CH2-Br
– Ngoài Brom, trong những điều kiện kèm theo thích hợp, etilen còn có phản ứng cộng vởi một số ít chất khác, như hiđro, …
Phản ứng trùng hợp của etilen C2H4
– Khi có xúc tác và nhiệt độ thích hợp, link kém bền trong phân tử etilen bị dứt ra làm cho những phân tử etilen tích hợp với nhau, tạo thành chất có phân tử lượng rất lớn gọi là polime .
…+ CH2=CH2 + CH2=CH2 + CH2=CH2 + … ![small xrightarrow[t^{0},P]{xt} Công thức cấu tạo của Etilen C2H4. Tính chất hoá học của etilen và bài tập 4](https://soanbaitap.com/wp-content/uploads/2020/03/giflatexsmallspacexrightarrowt0p_1548216818_1584140269.gif) …- CH2- CH2- CH2- CH2- CH2- CH2-…
…- CH2- CH2- CH2- CH2- CH2- CH2-…
– Phản ứng trên được gọi là phản ứng trùng hợp, polietilen ( PE ) là chất rắn, không độc, không tan trong nước và là nguyên vật liệu quan trọng trong công nghiệp chất dẻo .
III. Tính chất vật lý của Etilen C2H4
– Etilen là chất khí, không màu, không mùi, nhẹ hơn không khí và ít tan trong nước .
IV. Ứng dụng của Etilen C2H4
– Etilen dùng để sản xuất axit axetic, rượu etylic, poli ( vinyl clorua ), …
– Etilen dùng kích thích quả mau chín .
V. Bài tập về Etilen C2H4
Bài 1 trang 119 sgk hoá 9: Hãy tính số liên kết đơn, liên kết đôi giữa những nguyên tử cacbon trong phân tử các chất sau:
a ) CH3 – CH3 .
b ) CH2 = CH2 .
c ) CH2 = CH – CH = CH2 .
Lời giải bài 1 trang 119 sgk hoá 9 :
a ) CH3 – CH3 có 1 link đơn C – C .
b ) CH2 = CH2 có 1 link đôi : C = C .
c ) CH2 = CH – CH = CH2 có 2 link đôi : C = C và 1 link đơn : C – C .
Bài 3 trang 119 sgk hoá 9 : Hãy nêu phương pháp hóa học vô hiệu khí etilen có sẵn trong khí metan để thu được metan tinh khiết .
Lời giải bài 3 trang 119 sgk hoá 9 :
– Dẫn hỗn hợp qua dung dịch brom dư, khi đó etilen phản ứng tạo thành đibrometan là chất lỏng ở lại trong dung dịch và chỉ có metan thoát ra .
CH2 = CH2 + Br2 → Br – CH2 – CH2 – Br .
Bài 4 trang 119 sgk hoá 9 : Để đốt cháy 4,48 lít khí etilen cần phải dùng :
a ) Bao nhiêu lít oxi ?
b ) Bao nhiêu lít không khí chứa 20 % thể tích oxi ? Biết thể tích những khí đo ở điều kiện kèm theo tiêu chuẩn .
Lời giải bài 4 trang 119 sgk hoá 9 :
a ) Phương trình phản ứng cháy etien :
C2H4 + 3O2 → 2CO2 + 2H2 O .
– Theo bài ra, ta có : nC2H4 = 4,48 / 22,4 = 0,2 ( mol ) .
– Theo PTPƯ : nO2 = 3. nC2H4 = 3.0,2 = 0,6 ( mol ) .
⇒ VO2 = n.22,4 = 0,6.22,4 = 13,44 (lít).
Xem thêm: Thành tế bào – Wikipedia tiếng Việt
b ) Thể tích không khí = 13,44. ( 100 / 20 ) = 67,2 lít .
Công thức cấu tạo của Etilen C2H4. Tính chất hoá học của etilen và bài tập được biên soạn theo SGK Hóa học lớp 9 mới và được đăng trong mục giải hóa 9 và giải bài tập Hóa 9 gồm những bài Soạn Hóa 9 được hướng dẫn biên soạn bởi đội ngũ giáo viên dạy giỏi hóa tư vấn và những bài Hóa 9 được Soanbaitap. com trình diễn dễ hiểu, dễ sử dụng và dễ tìm kiếm, giúp bạn học giỏi hóa 9. Nếu thấy hay hãy san sẻ và comment để nhiều bạn khác học tập .
Source: https://sangtaotrongtamtay.vn
Category: Khoa học

Để lại một bình luận