Bạn đang đọc: Bảng tính tan hoá lớp 11 CHUẨN “Mẹo học thuộc nhanh bảng tính tan”">Bảng tính tan hoá lớp 11 CHUẨN “Mẹo học thuộc nhanh bảng tính tan”
3.9
/
5
(
30
bầu chọn
)
Khi bước vào lớp 8, các bạn học sinh sẽ phải làm quen với 1 môn học mới đó là môn hoá học. Ngoài các kiến thức quan trọng như nguyên tử khối, hoá trị thì bảng tính tan hoá học cũng là một trong những kiến thức quan trọng bắt buộc cần nhớ nếu muốn học tốt môn học này. Cùng tìm hiểu bảng tính tan đầy đủ nhất ngay sau đây.
I. Định nghĩa độ tan và ý nghĩa của bảng tính tan hoá học
1. Định nghĩa độ tan
Độ tan của 1 chất được hiểu là số gam chất đó có thể hoà tan trong 100g dung môi. Dung môi này thường là nước để tạo thành 1 dung dịch bão hoà ở điều kiện nhiệt độ nhất định. Và độ tan là đại lượng tượng trưng cho khả năng tan của 1 chất tại 1 điều kiện xác định.

Có nhiều yếu tố ảnh hưởng tác động đến độ tan của 1 chất như nhiệt độ, dung môi. Hoặc 1 số tác động ảnh hưởng như khuấy hoặc nghiền trộn nhỏ các chất cũng hoàn toàn có thể làm các chất tan nhanh hơn thường thì. Vì thế, nếu muốn xác lập độ tan 1 cách nhanh gọn thì các bạn hoàn toàn có thể sử dụng 1 số cách trên để quy trình tan được diễn ra nhanh hơn .
2. Ý nghĩa bảng tính tan hoá học
Bảng tính tan là 1 trong những công cụ không hề thiếu để xử lý các bài toán hoá học về độ kết tủa, độ tan, bay hơi hoặc nhận ra các chất trong phòng thí nghiệm 1 cách nhanh gọn. Do đó, các bạn cần bắt buộc phải ghi nhớ các kiến thức và kỹ năng này .
Để học thuộc bảng này không phải là điều thuận tiện, bởi trong này có rất nhiều quy tắc, các bạn hoàn toàn có thể tra cứu trong sách giáo khoa học bảng tính tan được in sẵn tại các hiệu sách. Nhưng các bạn hãy ghi nhớ để dữ thế chủ động xử lý và giải quyết và xử lý các bài toán hoá học và thao tác trong phòng thí nghiệm .
3. Yếu tố ảnh hưởng tác động độ tan
- Nhiệt độ, áp suất, thực chất của chất đó
- Các chất rắn thường phụ thuộc vào vào nhiệt độ, càng cao thì chất càng dễ tan ( ví dụ dễ thấy khi hòa tan đường vào nước )
- Với chất khí độ tan lại nhờ vào khi tăng nhiệt độ và tăng áp suất
II. Bảng tính tan lớp 11 và các lớp tương quan
Trong chương trình hóa học trung học cơ sở, các bạn đã được học bảng tính tan lớp 9. Tuy nhiên, bảng tính tan hóa học 11 sẽ phức tạp hơn so với bảng tính tan sgk lớp 9 và các bạn sẽ được học tiếp nội dung này, nhưng với các nội dung nâng cao hơn .
1. Bảng tính tan hoá học
Bảng tính tan trong môn hóa học đã khởi đầu được học và có từ lớp 8. Do đó cái tên bảng tính tan Hóa 8 là cái tên quen miệng của nhiều bạn học viên. Và đây cũng chính là bảng tính tan vận dụng trong suốt những năm đi học .
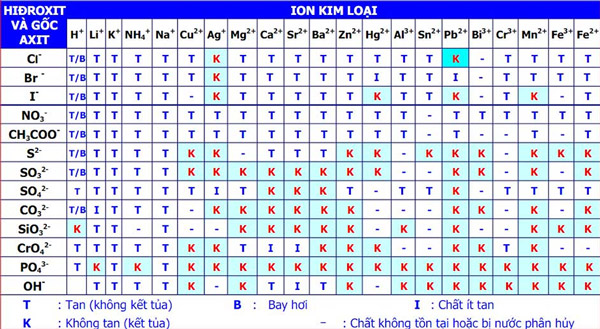
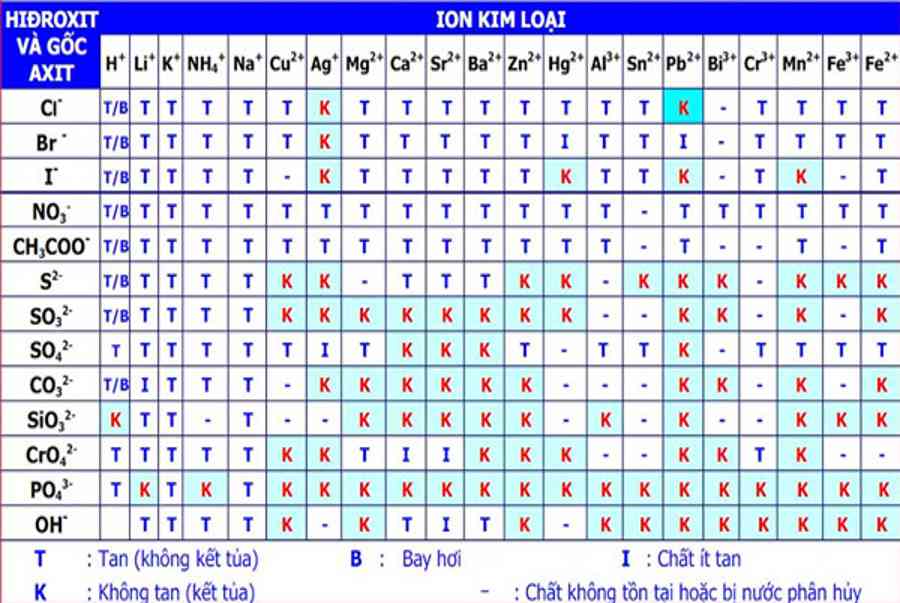
Bảng tính tan hóa học đầy đủ có các ký hiệu như sau:
- I : chất ít tan
- K : chất không tan
- T : chất dễ tan
- B : chất bay hơi
- – : Chất bị nước phân huỷ hoặc chất không sống sót .
Không có một QUY LUẬT bảng tính tan nào cả. Vậy nên cách duy nhất để nhớ là làm nhiều bài tập và sử dụng nhiều đến nó .
2. Cách đọc bảng tính tan
Bảng tính tan hoá học gồm có các cột và các hàng ( các bạn học viên hoàn toàn có thể tìm tại Bảng tính tan SGK Hóa 9 ). Hàng là anion gốc axit ( OH – ), còn cột là các cation sắt kẽm kim loại. Đối với 1 số chất đơn cử thì ta sẽ xác lập được ion âm và ion dương, gióng theo các cột và hàng tương ứng ta sẽ biết được trạng thái của chất đó .
>> > Tìm hiểu thêm : bảng tuần hoàn hoá học vừa đủ nhất
III. Mẹo học thuộc nhanh bảng tính tan
Trong quá trình học hoá, các bạn cần thực hành và làm nhiều bài tập để có thể dễ dàng nhớ về khả năng hòa tan cũng như điều kiện hoà tan của các hợp chất. Điều này sẽ giúp các bạn có thể hiểu sâu thêm về bản chất của các phản ứng hoá học và dễ dàng nhớ được độ tan của các chất thường gặp trong bảng tính tan.
Tuy nhiên, việc học thuộc bảng tính tan vừa đủ sẽ không phải là điều thuận tiện và liên tục bị nhầm lẫn. Dưới đây là 1 số chiêu thức, cách học thuộc bảng tính tan nhanh gọn đã được nhiều bạn vận dụng thành công xuất sắc như sau :

1. Quy tắc rút gọn về tính tan
Cách nhớ bảng tính tan mưu trí bằng quy tắc rút gọn, đơn cử như thế nào mới bạn đọc theo dõi nội dung tiếp theo đây .
Tính tan đối với muối:
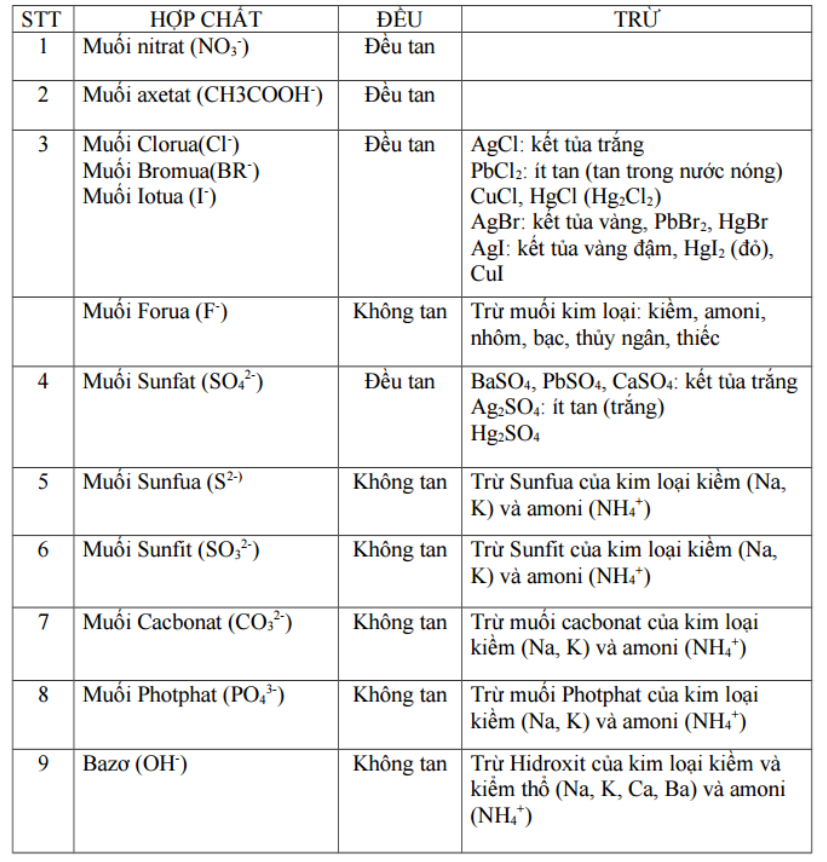
Các muối tan và không tan được tổng hợp đơn cử và đúng mực. Tính tan của muối như sau
- Muối có gốc halogen như Cl, Br, F, đa số đều tan được trong nước và điều đặc biệt quan trọng khi bạn tính năng với các nguyên tố trong nhóm này thì sẽ không tan mà sẽ tạo ra kết tủa với màu đặc trưng. Nắm rõ bảng tính tan và màu kết tủa cũng là một trong những cách để nhận ra các nguyên tố nhóm halogen .
-
Muối gốc Silicat ( SiO3), sunfit ( SO3) không tan trong nước. Tuy nhiên, so với các sắt kẽm kim loại mang tính kiềm và các muối có các gốc trên vẫn tan được trong nước. Nói chung, các sắt kẽm kim loại kiềm sau khi tích hợp với các hợp chất khác tạo ra muối thì đều có năng lực tan trong nước. Bạn hãy nhìn vào bảng tính tan, muối của các sắt kẽm kim loại này sẽ được lưu lại chữ t .
-
Muối cacbonat ( CO3) phần nhiều không tan được trong nước. Nhưng các sắt kẽm kim loại đứng đầu trong bảng tuần hoàn hoá học có tính kiềm như K, Na, Li, .. sẽ tan được trong nước. Do đó, bạn hoàn toàn có thể nhìn vào bảng tính tan vừa đủ và sẽ thấy được lưu lại chữ t, tức là hợp chất muối này hoàn toàn có thể hoà tan được trong môi trường tự nhiên nước .
-
Muối gốc sunfua ( S ) đều khó tan trừ các sắt kẽm kim loại thuộc nhóm 1 và nhóm 2 trên bảng tuần hoàn như K2S, BaS, Na2S hoàn toàn có thể tan trong nước .
- Muối gốc SO4 phần đông đều tan trong nước và trừ muối sunfat của sắt kẽm kim loại bari không tan .

Lưu ý, có 1 số muối không sống sót hoặc nó hoàn toàn có thể bị phân huỷ ngay trong nước. Các muối này được ký hiệu bằng dấu “ – ” trên bảng tính tan và trường hợp này không nhiều nên các bạn hoàn toàn có thể thuận tiện học .
Tính tan đối với axit và bazo:
Các hợp chất axit đều thuận tiện tan được trong nước. Riêng so với H2CO3 có link bền và thuận tiện bị phân huỷ trong nước. Một hợp chất axit duy nhất không tan trong nước chính là H2SiO3 .
Các bazo phần đông không tan trong nước, riêng so với sắt kẽm kim loại bazơ kiềm như Li, K, N sẽ tan trong nước. Còn các bazo của sắt kẽm kim loại nhóm 2 thì tan ít trong nước .
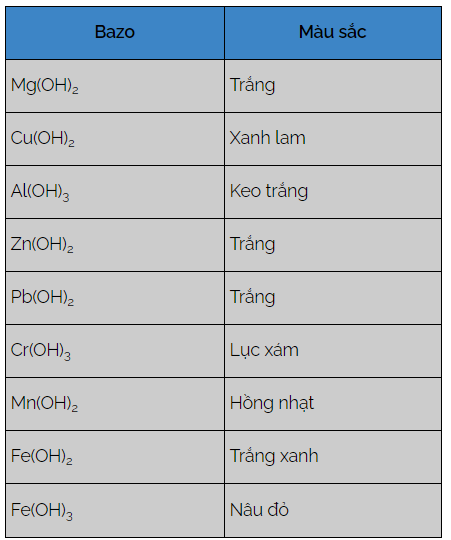
Bảng tính tan được coi như là kỹ năng và kiến thức nền tảng của môn hoá học để các bạn hoàn toàn có thể học tốt hơn sau này. Do đó, hãy cần mẫn và tiếp tục làm bài tập để hoàn toàn có thể hiểu sâu được yếu tố nhé !
2. Thực hành liên tục
Cách thuộc bảng tính tan là thực hành thực tế đi thực hành thực tế lại. Nếu trường học của bạn có điều kiện kèm theo thì việc tiếp tục đến phòng thực hành thực tế sẽ giúp các bạn học tốt môn hoá học rất nhiều. Cốt lõi của môn hoá học là nắm rõ thực chất của phản ứng hoá học. Khi triển khai thí nghiệm sẽ giúp bạn tận mắt nhìn thấy các phản ứng và điều kiện kèm theo để xảy ra phản ứng .
Cách học bảng tính tan là hãy làm bài tập nhiều. Thực hành nhiều sẽ giúp bạn thuộc tính tan của 1 số chất hay sử dụng. Điều này khiến cho bảng tính tan trở nên quen thuộc và dễ nhớ hơn rất nhiều .
Trong chương trình hoá học ở trung học cơ sở các bạn sẽ được học sơ lược về hoá học. Những kiến thức này sẽ là tiền đề cho môn hoá học ở bậc phổ thông.
3. Cách học thuộc nhanh bảng tính tan ghi nhớ bằng hình ảnh
Hình ảnh khiến mọi thứ ghi nhớ trở nên nhanh gọn .

Bảng tính tan có thể được coi là 1 trong những kiến thức gốc của hoá học. Do đó, muốn nhớ được thì các bạn cần phải có phương pháp và thái độ học tập chuyên tâm. Nếu chỉ học vẹt, học 1 cách vô thức thì các kiến thức cũng chỉ vào trước, ra sau và không đem lại hiệu quả thực sự. Hy vọng với những chia sẻ bên trên sẽ giúp ích được các bạn trong quá trình học tập về bảng tính tan hoá học. Chúc các học tốt ở môn học này.
Xem thêm các kỹ năng và kiến thức quan trọng khác :
Source: https://sangtaotrongtamtay.vn
Category: Giáo dục