Nguyên tử là đơn vị cơ bản của vật chất, có vai trò quan trọng đối với đời sống cũng như quá trình nghiên cứu trong nhiều lĩnh vực. Hãy cùng tìm hiểu nguyên tử là gì, cấu tạo và tính chất trong bài viết sau đây nhé!
Xem Tóm Tắt Bài Viết Này
Nguyên tử là gì?
Nguyên tử là đơn vị chức năng cơ bản của vật chất, được xác lập bởi cấu trúc của những nguyên tố. Nguyên tử gồm có một hạt nhân ở TT, được bảo phủ bởi đám mây điện tích âm electron .
Nguyên tử có size rất nhỏ với đường kính chỉ bằng khoảng chừng vài phần mười của nano mét. Ký hiệu nguyên tử là Z, xuất phát từ tiếng Đức Zahl có nghĩa là số .
Cấu tạo của nguyên tử
Nguyên tử được cấu tạo từ 3 loại hạt là proton, electron và neutron. Trong đó, proton và neutron có khối lượng nặng hơn electron rất nhiều và thường nằm trong tâm của nguyên tử (hạt nhân). Còn electron có khối lượng cực nhẹ và tồn tại trong 1 đám mây bao quanh hạt nhân với bán kính lớn gấp 10000 lần hạt nhân.
Bạn đang đọc: Nguyên tử là gì? Cấu tạo của nguyên tử">Nguyên tử là gì? Cấu tạo của nguyên tử
Proton và neutron có khối lượng xê dịch nhau, trong đó một proton có khối lượng khoảng chừng 1800 electron. Các nguyên tử cấu thành nên những trạng thái vật chất khác nhau. Tùy thuộc vào những điều kiện kèm theo vật lý như nhiệt độ, tỷ lệ, áp suất, thì sẽ dẫn đến sự chuyển pha vật chất giữa khí, lỏng, rắn và plasma .
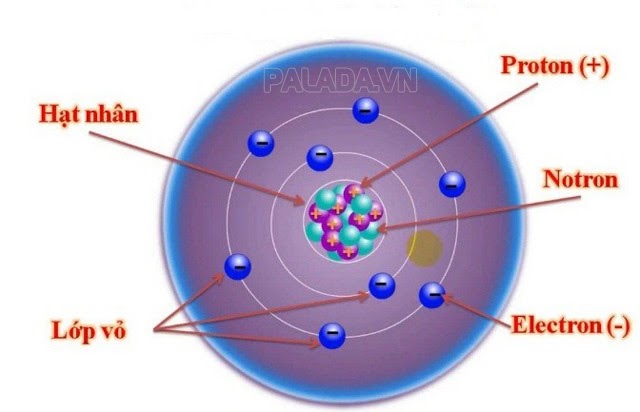
Proton
Proton là hạt mang điện tích dương và được tìm thấy trong hạt nhân của nguyên tử. Số lượng proton sẽ giúp xác lập được nguyên tử này là nguyên tố gì. Ví dụ, nguyên tử Cacbon có 6 proton, nguyên tử Hydro có 1 proton và nguyên tử Oxy có 8 proton. Số lượng proton trong 1 nguyên tử được gọi là số nguyên tử của nguyên tố này .
Notron
Neutron là hạt không mang điện tích và được tìm thấy trong hạt nhân của nguyên tử. Khối lượng của 1 notron thường lớn hơn khối lượng của 1 proton .
Electron
Electron là hạt mang điện tích âm và sẽ bị hút về proton có điện tích dương. Các electron bao quanh hạt nhân của nguyên tử được gọi là orbital. Các orbital bên trong nguyên tử có dạng hình cầu, còn orbital bên ngoài thì phức tạp hơn .
Dựa trên việc sử dụng thông số kỹ thuật electron và nguyên tắc vật lý, những nhà hóa học hoàn toàn có thể Dự kiến được đặc thù của 1 nguyên tử như độ không thay đổi, độ dẫn, điểm sôi, …
Nguyên tử khối là gì?
Nguyên tử khối là khối lượng của nguyên tử được tính bằng đơn vị chức năng cacbon ( đvC ). 1 đvC có giá trị bằng 1/12 khối lượng của 1 nguyên tử cacbon. Khối lượng nguyên tử được tính bằng gam hoặc kilogam và có trị số rất nhỏ .
Khối lượng của 1 nguyên tử cacbon bằng ( 1,6605 ). 10 ^ ( – 24 ) g. Từ đó suy ra, 1 đvC = ( 1/12 ). 1,9926. 10 ^ ( – 23 ) = 1,6605. 10 ^ ( – 24 ) g .
Phân tử là gì?
Phân tử là một nhóm trung hòa điện tích, có từ 2 nguyên tử trở lên, được phối hợp bằng những link hóa học. Các phân tử thường được phân biệt với những ion do thiếu điện tích .
Tuy nhiên, trong vật lý lượng tử, hóa hữu cơ và hóa sinh, phân tử được sử dụng cho những ion đa nguyên tử. Còn trong triết lý động học của chất khí, phân tử được sử dụng cho toàn bộ những loại hạt khí, bất kể thành phần, gồm có cả những nguyên tử khí trơ .
Phân tử khối là gì?
Phân tử khối là khối lượng của một phân tử được tính bằng đơn vị chức năng cacbon. Phân tử khối của một chất bằng tổng nguyên tử khối của những nguyên tử có trong phân tử của chất đó. Ví dụ, phân tử khối của Oxy ( O2 ) bằng 16.2 = 32 đvC .
Hạt nhân nguyên tử là gì?
Được cấu tạo bởi các neutron và proton, trong hạt nguyên tử, số proton (p, +) bằng số electron (e, -). (số p= số e). Hạt proton và neutron có khối lượng tương đương, còn hạt electron có khối lượng rất nhỏ, không đáng kể. Chính vì thế, khối lượng hạt nhân thường được coi là khối lượng nguyên tử.
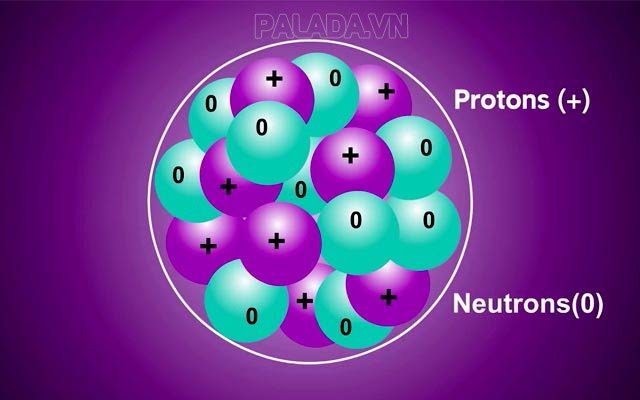
Số nguyên tử là gì?
Số nguyên tử ( hay còn gọi là số hiệu nguyên tử ) là số proton được tìm thấy trong hạt nhân của một nguyên tử, tựa như số điện tích của hạt nhân. Mỗi nguyên tố hóa học có một số ít nguyên tử xác lập duy nhất. Nếu một nguyên tử không tích điện thì số lượng nguyên tử bằng với số electron .
Nguyên tố hóa học là gì?
Nguyên tố hóa học là một chất hóa học, gồm có những nguyên tử có cùng số proton có trong hạt nhân ( hay còn gọi là số hiệu nguyên tử ) với những kí hiệu hóa học khác nhau để phân biệt .
Công thức tính phân tử khối của hợp chất
Ta có, đơn chất sắt kẽm kim loại và phi kim ở dạng rắn : Ax ( x = 1 ). Trong đó, A là nguyên tố, x là số nguyên tử có trong phân tử của chất đó. Đơn chất phi kim ở dạng khí là : Ax ( x = 2 ) .
Công thức hóa học của hợp chất gồm có hai hay nhiều kí hiệu hóa học kèm theo chỉ số AxByCz. Trong đó : A, B, C là ký hiệu hóa học của những nguyên tố ; x, y, z là số nguyên tố có trong 1 phân tử .
Phân tử khối của hợp chất bằng tổng khối lượng của nguyên tử có trong phân tử, tính theo đơn vị chức năng cacbon ( đvC ). Ví dụ, phân tử khối của muối ( NaCl ) = 23 + 35,5 = 58,5 đvC .
Cách tính nguyên tử khối
3 bước tính nguyên tử khối những chất :
Bước 1 : Ghi nhớ giá trị 1 đvC = 1,6605. 10-27 kg = 1,6605. 10-24 g
Bước 2 : Tra bảng nguyên tử khối hóa học của nguyên tố. Ví dụ, nguyên tố A có nguyên tử khối là a, A = a .
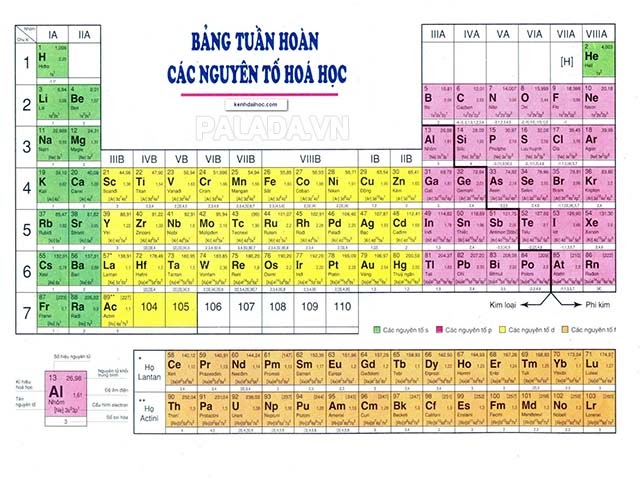
Bước 3 : Khối lượng thực của A là : mA = a. 0,166. 10-23 = ? ( g )
Ví dụ, bạn có 16 g Oxi, hỏi có bao nhiêu nguyên tử Oxy trong 16 g này ?
16 g là khối lượng được tính bằng gam tương ứng với số nguyên tử. Áp dụng công thức tính nguyên tử khối, ta có :
Số nguyên tử = Khối lượng tính bằng gam / Khối lượng tính bằng gam của 1 nguyên tử
=> Số nguyên tử có trong 16g Oxy là: 16/(16.1,6605.10-24) = 6,02.10-23
1 mol oxy có khối lượng 16 g = 16 ( đvC ) => 1 nguyên tử oxy có khối lượng là 16.1,6605. 10 ^ ( – 24 ) ( g )
Tương tự, tất cả chúng ta hoàn toàn có thể thuận tiện tính được nguyên tử khối của những chất Ba, Na, Cu, C ( Cacbon ), P. ( Photpho ) …
Trên đây là tổng hợp kỹ năng và kiến thức tương quan đến nguyên tử. Hy vọng những san sẻ trong bài viết đã giúp những bạn biết được cách giải bài tập về nguyên tử lớp 8 và ứng dụng thành công xuất sắc trong học tập .
Source: https://sangtaotrongtamtay.vn
Category: Khoa học